Tetraploide Embryo-Komplementierung
Das Verfahren der tetraploiden Embryo-Komplementierung dient dem Nachweis der Pluripotenz von Stammzellen. Bei dem Verfahren werden die Zellen eines Embryos im Zweizellstadium durch Zellfusion zu einer einzigen Zelle zusammengefügt. Aus zwei Zellen wird so eine Zelle mit einem doppelten diploiden Chromosomensatz. Die daraus entstehenden Zellen sind aufgrund des nunmehr tetraploiden, d.h. vierfachen Chromosomensatzes nicht mehr in der Lage, einen vollständigen Organismus auszubilden, sondern können sich lediglich zu Zellen des Trophoblasten, also zur Hüllschicht des Embryos im Blastozystenstadium, aus der später Plazenta und Nabelschnur hervorgehen, ausdifferenzieren. Um einen lebensfähigen Organismus zu bilden, braucht es jedoch auch die innere Zellmasse der Blastozyste, den Embryoblasten. Die Zellen des Embryoblasten differenzieren sich im Verlauf der Embryogenese in alle Gewebearten eines Organismus und bilden daher den eigentlichen Embryo. Ergänzt man die wie oben beschrieben gewonnenen Trophoblastzellen durch embryonale oder induzierte pluripotente Stammzellen (dieser Vorgang wird auch „sandwichen” genannt) entsteht aus diesen ein entwicklungsfähiger Embryo.
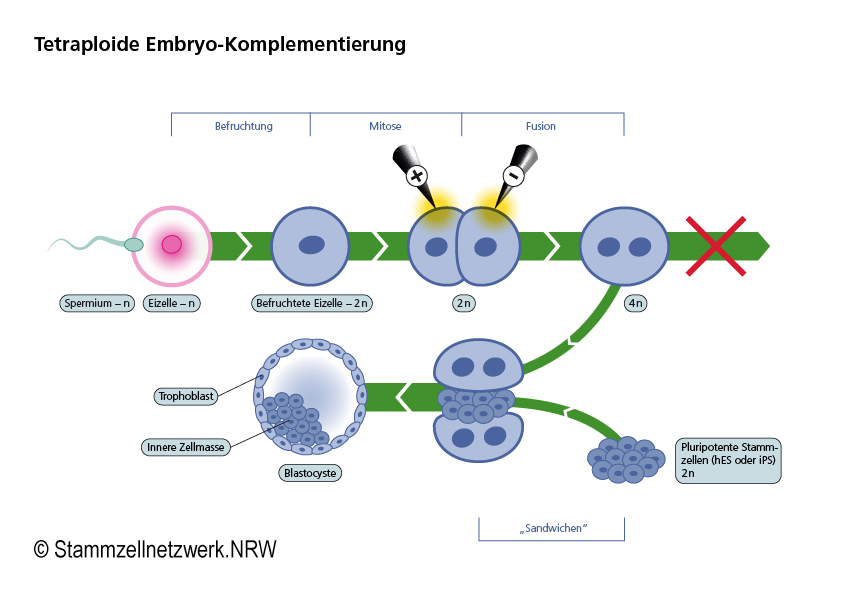
Bei frühen Experimenten, die mit ES-Zellen durchgeführt wurden, fanden sich einige der eingebrachten pluripotenten Stammzellen später nicht nur im Embryoblasten, sondern auch im Trophoblasten wieder. Einige Forschende sprechen daher in diesem Zusammenhang von einer Totipotenz dieser speziellen Zellen im eingeschränkten Sinne.
Mit dem Verfahren konnte am Mausmodell gezeigt werden, dass aus induzierten pluripotenten Stammzellen (iPS-Zellen) vollständige Organismen entstehen können. Michael J. Boland, Jennifer L. Hazen und Kristopher L. Nazor vom Scripps Research Institute veröffentlichten im September 2009 eine Studie im Fachmagazin Nature, bei der es unter Verwendung von murinen Fibroblastzellen gelungen war, den Nachweis zu erbringen, dass iPS-Zellen sich in jedweden Zelltyp und unter Zuhilfenahme des Verfahrens der tetraploiden Embryo-Komplementierung zu einem vollständigen Organismus entwickeln können. Dazu wurden zunächst Zellen eines Embryos durch Zellfusion zusammengefügt. Den tetraploiden Zellen wurden dann, mithilfe der iPS-Technologie gewonnene, pluripotente Stammzellen hinzugefügt, die in der Folge die innere Zellmasse der Blastozyste, den Embryoblast, bildeten. Diese nunmehr kompletten Embryonen wurden anderen Mäusen zum Austragen transferiert. Sie wuchsen zum Teil zu lebensfähigen Mäusen heran und kamen zur Welt. Ein wesentliches Hindernis bis dahin etablierter Klonierungstechniken, die limitierte Effizienz des Kerntransfers, wird bei der tetraploiden Komplementierung umgangen.
Ursprünglich wurde das Verfahren der tetraploiden Embryo-Komplementierung entwickelt, um transgene „Knockout”-Mäuse auszutragen. (Siehe dazu auch den Blickpunkt „Tierversuche in der Forschung”. Online Version)
Link zur Studie:
Boland, M. J., Hazen J. L., Nazor, K. L., Rodriguez, A. R., Gifford, W., Martin, G., Kupriyanov, S., & Baldwin, K. K.(2009). Adult mice generated from induced pluripotent stem cells. In Nature 461(7260): 91–4. https://doi.org/10.1038/nature08310
Zur weiteren Information:
Sgodda, S. (2014). Das Kriterium der Totipotenz aus naturwissenschaftlicher Perspektive. In Heinemann, T., Dederer, H., & Cantz, T. (2014). Entwicklungsbiologische Totipotenz in Ethik und Recht: Zur normativen Bewertung von totipotenten menschlichen Zellen. Vandenhoeck & Ruprecht.
Zhao, X., Li, W., Lv, Z., Liu, L., Tong, M., Hai, T., Hao, J., Guo, C., Ma, Q., Wang, L., Zeng, F., & Qi Z. (2009). iPS cells produce viable mice through tetraploid complementation. In Nature 461, 86–90. https://doi.org/10.1038/nature08267
Kang, L., Wang, J., Zhang, Y., Kou, Z., & Gao, S. (2009). iPS Cells Can Support Full-Term Development of Tetraploid Blastocyst-Complemented Embryos. In Cell Stem Cell 5 (2), 135–138. https://doi.org/10.1016/j.stem.2009.07.001