Virale Vektoren
Viren sind infektiöse Partikel, die aus einer Nukleinsäure (DNA oder RNA) und einer Proteinhülle bestehen. Da sie selbst keine Stoffwechselvorgänge durchführen, erfolgt die Fortpflanzung von Viren über die Einbringung des eigenen Erbguts in die Zellen eines Wirts und die Manipulation der Wirtszelle zur Produktion weiterer Viren.
Für den Einsatz in gentherapeutischen Studien sind vor allem zwei Arten von Viren geeignet: Retroviren, wie Alpharetroviren, Gammaretroviren, Spumaretroviren oder Lentiviren, integrieren das transportierte Erbgut direkt in das Genom der Zielzelle. Adeno- oder Herpesviren erstellen hingegen ein eigenständiges Element außerhalb des Genoms (Episom), welches bei der Zellteilung nicht repliziert wird und daher nach einiger Zeit wieder verloren geht.
Um ein Virus als Vektor nutzbar zu machen, muss es zunächst genetisch so modifiziert werden, dass nach Einbringung des genetischen Materials keine Virusvektorpartikel gebildet werden (replikationsdefekte Form). Zu diesem Zweck werden die entsprechenden viralen Sequenzen des Erbmaterials entfernt, sodass nur jene zur Einbringung und Integration des gewünschten Materials in das Genom der Zielzelle erhalten bleiben.
Die Einbringung des genmodifizierten Materials mithilfe viraler Vektoren in die Zielzelle (Transduktion) kann entweder direkt im Organismus (in vivo) oder an zuvor entnommenen Zellen desselben (ex vivo) erfolgen. Letzteres bietet zwar den Vorteil, dass eine mögliche Keimbahntransmission ausgeschlossen wird, jedoch ist die ex vivo Gentherapie auf Zellen beschränkt, die relativ leicht aus dem Körper der zu behandelnden Person extrahiert und anschließend repliziert werden können. Zudem besteht die Gefahr, dass eine Reimplantation der modifizierten Zellen nur unvollständig gelingt.
Zur Einschätzung der Potenz und der Sicherheit viraler Vektoren ist im Wesentlichen die Zahl der im Produktionsprozess erzeugten infektiösen Partikel, der Optionen für die Gestaltung der Partikeloberfläche zur selektiven Aufnahme in die jeweiligen Zielzellen, die Größe und der Aufbau des übertragbaren genmodifizierten Materials, die Möglichkeit der Elimination viruscodierender Gensequenzen sowie die immunogenen oder toxikologischen Eigenschaften der viralen Proteine, die im Vektorpartikel benötigt werden, von Bedeutung. Zudem muss eine frühere Infektion der zu behandelnden Person mit immunologisch verwandten Viren ausgeschlossen werden, um eine Immunreaktion zu verhindern.
Weiterführende Informationen:
Baum, C. (2013): Medizinisch-naturwissenschaftliche Aspekte. In: Baum, C. / Duttge, G. / Fuchs, M.: Gentherapie. Medizinisch-naturwissenschaftliche, rechtliche und ethische Aspekte. Bd. 15 der Reihe Ethik in den Biowissenschaften – Sachstandsberichte des DRZE. Freiburg i. B.: Verlag Karl Alber, 16–22.
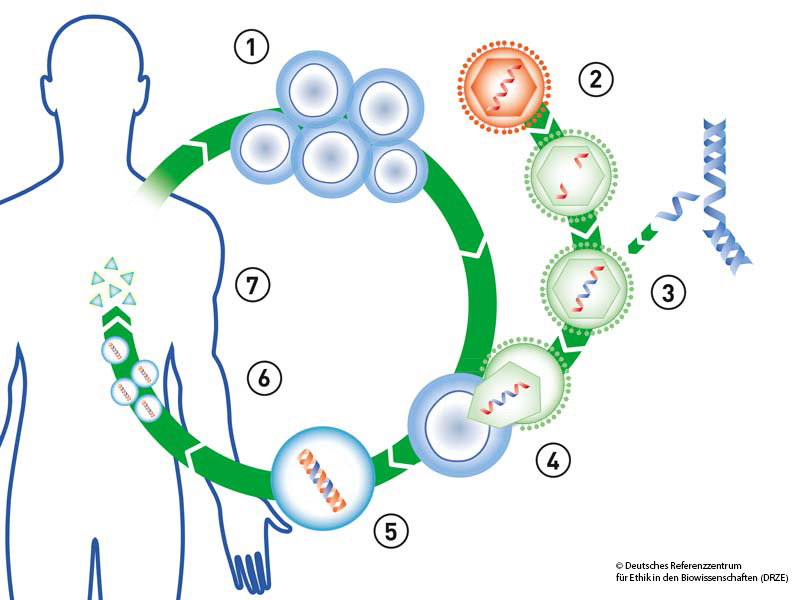
Abbildung: 1. Entnahme von Zellen; 2. Modifikation des Virus; 3. Einbringung des gewünschten Genmaterials; 4. Einschleusen des intakten Genmaterials mithilfe des Virus; 5. Vermehren der Zellen mit dem korrigierten Gen; 6. Infusion der gentherapeutisch veränderten Zellen; 7. Die gentherapeutisch veränderten Zellen produzieren das gewünschte Protein oder die gewünschten Hormone, die zuvor nicht produziert werden konnten.
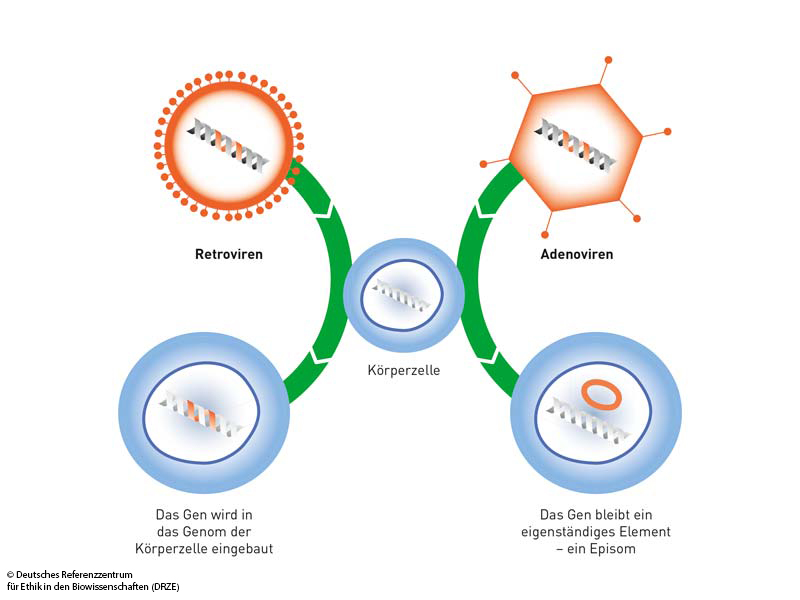
Abbildung: Virale Vektoren: Retroviren und Adenoviren